Technical
| Begriff | Definition |
|---|---|
| Feldspat | Als Feldspat wird eine große Gruppe sehr häufig vorkommender Silikat-Minerale der allgemeinen chemischen Zusammensetzung (Ba,Ca,Na,K,NH4)(Al,B,Si)4O8 bezeichnet. Die in Klammern angegebenen Elemente können sich jeweils gegenseitig vertreten, stehen jedoch immer im selben Mengenverhältnis zu den anderen Bestandteilen des Minerals (Substitution). Feldspate kristallisieren entweder im monoklinen oder im triklinen Kristallsystem, haben eine mittlere Mohshärte von 6 bis 6½ und eine sehr variable Farbe, die von farblos über weiß, rosa, grün, blau bis braun reicht. Die Strichfarbe ist weiß. Feldspate gelten als die wichtigsten gesteinsbildenden Minerale der Erdkruste. Der Schmelztemperaturbereich liegt bei 1150–1250 °C.[1]
Zugriffe - 1596
|
| Filterkuchen | Filterkuchen bezeichnet den Rückstand aus zurückgehaltenen Stoffen in einer Kammerfilterpresse. Kammerfilterpressen werden auch bei der Herstellung von Lebensmitteln, beispielsweise beim Winemaking, eingesetzt. Weinhefe beschreibt dort den Charakter des Filterkuchens eindeutig. Bei der Verwitterung der Gesteine des ca. 400 Millionen Jahre alten Rheinischen Schiefergebirges entstanden im Westerwald durch Erosion mittels Wasser große und vereinzelt am Hunsrück- und Taunussüdrand kleine Tonvorkommen. Diese bestehen aus sehr feinkörnigen Komponenten, überwiegend mit einer Korngröße von unter 0,002 mm. Im Steinbruch Sooneck wird dieser Verwitterungsprozess im Zeitraffer nachvollzogen. Nach dem Sprengen werden die feinsten Fraktionen durch Siebe trocken abgetrennt. In der Nassaufbereitung werden mittels Wasser die Korngrößen von unter 0,002 mm aufkonzentriert, dabei aber auch der Quarzgehalt abgesenkt. Um das Wasser wieder nutzen zu können, wird der Rheinstein-Ton in einer Kammerfilterpresse auf einen für die Kunden optimalen Wassergehalt entwässert und wiederverwendet. Dabei gewährleistet eine fortlaufende Qualitätskontrolle, dass mit dem Rheinstein-Ton ein Produkt für Baustoffe mit den für die verschiedenen Einsatzmöglichkeiten besten Eigenschaften entsteht und zugleich eine Bodenverbesserung erreicht wird.
Zugriffe - 1514
|
| Flugasche | Flugasche ist der feste, disperse (teilchenförmige, partikelförmige, staubförmige) Rückstand von Verbrennungen, der auf Grund seiner hohen Dispersität (Feinverteilung) mit den Rauchgasen ausgetragen wird. Flugasche entsteht in großen Mengen in Wärmekraftwerken und Müllverbrennungsanlagen und muss dort durch Entstauber aus den Rauchgasen abgeschieden werden. Die Partikelgröße reicht von etwa 1 µm bis 1 mm. An Partikelformen treten sowohl glatte, massive Kugeln als auch Hohlkugeln (sogenannte Cenosphären), Plättchen, Fasern und Agglomerate auf. Die Dichte beträgt 2,2 bis 2,4 kg/l, die Schüttdichte liegt zwischen 0,9 und 1,1 kg/l. Die Zusammensetzung der Flugasche hängt stark vom Brennmaterial (zum Beispiel Braunkohle oder Steinkohle) ab und erstreckt sich von Restkohlenstoff und Mineralien (Quarz, Aluminiumsilikat) bis hin zu toxischen Stoffen wie Schwermetallen (Arsen bis Zink) und Dioxinen. Dabei wirkt die Flugasche auch als Träger adsorbierter Schadstoffe. Während reine, einheitliche, gleichbleibende Brennstoffe wie Steinkohle eine gut verwertbare Flugasche ergeben, setzt sich die Braunkohlenflugasche (BFA) aus vielen verschiedenen Stoffen zusammen.
Zugriffe - 1771
|
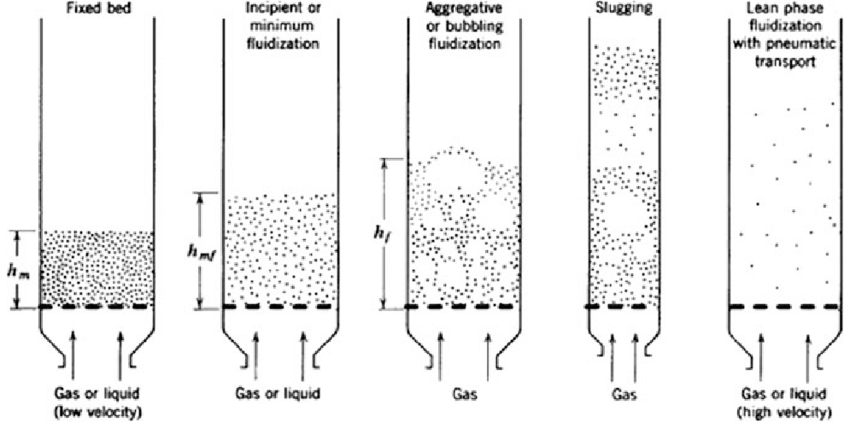
| Fluidschema |
Zugriffe - 1639
|
| Funktionelle Gruppen | Unter einer funktionellen Gruppe versteht man die Verbindungen, die die Stoffeigenschaften und das Reaktionsverhalten ihrer Atomgruppen beeinflussen. Somit bestimmen diese Atome die „Funktion“ des jeweiligen Stoffes. Auch einfache Alkyl- oder Aryl-Gruppen können als funktionelle Gruppen angesehen werden. Organische Verbindungen werden in Stoffklassen eingeteilt. Grundlage dieser Stoffklassen ist immer das Kohlenstoffgerüst, abgeleitet von einem Stamm-Moleküle, einem Stamm-Kohlenwasserstoff. Durch Ersatz (=Substitution) von einem oder mehreren Wasserstoff-Atomen durch andere Atome oder Atomgruppen entstehen Derivate (=Abkömmlinge) der Kohlenwasserstoffe (=KW). Der KW-Rumpf stellt den Stammkörper des Derivats dar, die eingeführten Atome oder Atomgruppen nennt man funktionelle Gruppen. Die funktionellen Gruppen bestimmen Eigenschaften und Reaktionsverhalten von Verbindungen; durch die funktionelle Gruppe wird eine Stoffklasse gebildet, z.B. R-OH, wobei R- für den KW-Rest steht und -OH die funktionelle Gruppe ist. Die Stoffklasse R-OH stellt die Stoffklasse der Alkohole dar.
Mit der Zunahme der Pyrolysetemperaturen gehen immer mehr funktionelle Gruppen weg. D.h. die O- und H-Anteile für solche Gruppen lösen sich mehr und mehr auf. Interessant ist aber, dass PK z. B. im Boden durch die Alterung erneut mit funktionellen Gruppen aus der Umgebung besetzt wird. Sie wird damit reaktiver und die Bindungskraft scheint zuzunehmen.
Zugriffe - 1625
|
| Funktionelle Gruppen II | Den funktionellen Gruppen entsprechend teilt man organische Verbindungen ein in
Daneben gibt es organische Salze, z. B. Hydrochloride und Hydrobromide. Als Verbindungen der per Definition anorganischen Kohlensäure (H2CO3) zählen Carbonate jedoch nicht dazu.
Zugriffe - 1615
|
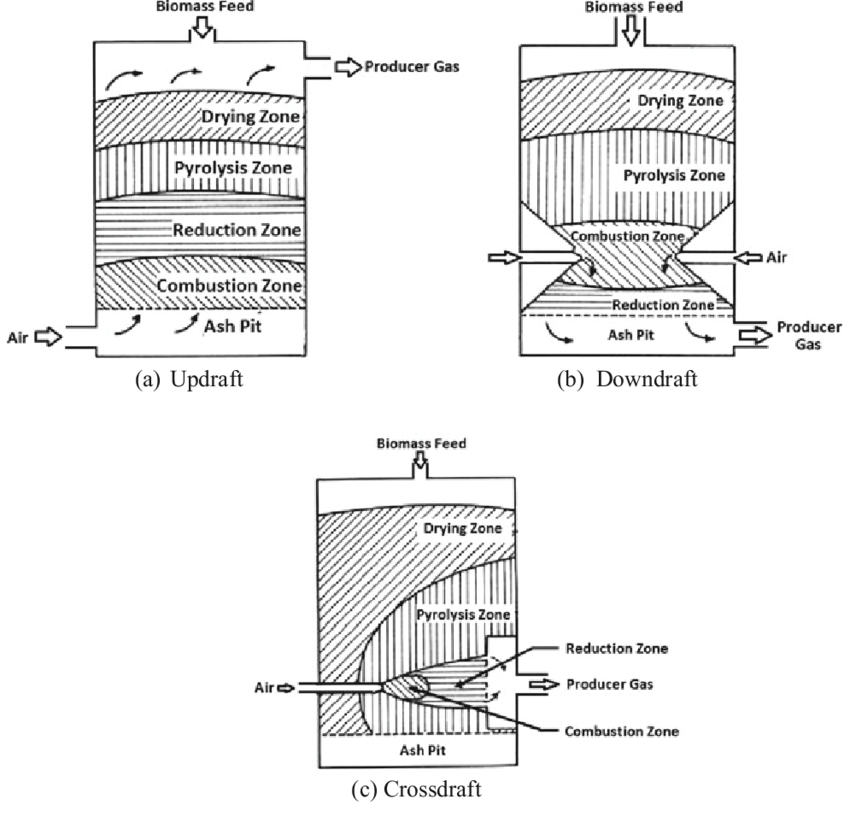
| Gas-Wege |
Zugriffe - 1721
|
| Gesättigt | n der organischen Chemie bezeichnet gesättigte Verbindung eine Gruppe von Stoffen, in denen alle Bindungen zwischen Kohlenstoffatomen eines Moleküls Einfachbindungen sind. Alle Valenzen der Kohlenstoffatome sind ausgeschöpft, es können durch Additionsreaktionen keine zusätzlichen Atome oder Atomgruppen aufgenommen werden.[1] Gesättigte Kohlenwasserstoffe werden in der Chemie als Alkane bezeichnet. Einen Sonderfall stellen komplexe zusammengesetzte Verbindungen dar (zum Beispiel Verbindungen, die aus mehreren Ringen bestehen, etwa Propiconazol), bei denen sich die Bezeichnung nur auf Teile der Verbindung (z. B. einzelne Ringe) beziehen kann. Eigenschaften[Bearbeiten | Quelltext bearbeiten]Gesättigte Verbindungen sind in der Regel stabiler und weniger reaktiv als ungesättigte Verbindungen, da keine sterischen Hinderungen und keine großen Polaritätsunterschiede auftreten. Außerdem besitzen sie im Verhältnis zur Molmasse recht niedrige Schmelz- und Siedepunkte.
Zugriffe - 1631
|
| Graphitentstehung/Herstellung | Bei einer Temperatur von über 2500 °C wird Graphit plastisch verformbar und sublimiert in einer sauerstofffreien Umgebung bei einer Temperatur von 3750 °C.[14] Unter Sauerstoffeinwirkung entzündet sich Graphit bei etwa 600 °C.[15] Graphit ist beständig gegen nichtoxidierende Säuren und ist diamagnetisch. Auffällig ist das stark anisotrope Verhalten von Graphit, insbesondere hinsichtlich Härte und elektrischer Leitfähigkeit.
Nach der Entstehung wird Graphit in drei Arten eingeteilt: Flockengraphit (flake graphite), amorphen Graphit (amorphous graphite) und Ganggraphit (vein graphite). Der Flockengraphit ist die häufigste Graphitvariante, er besteht aus Plättchen und kommt in metamorphen Gesteinen, wie z. B. Marmor, Gneis oder Schiefern, vor. Der amorphe Graphit ist ein sehr feinkörniger Graphit, der in Kohleflözen, Tonsteinen und Schiefern vorkommt. Der Ganggraphit ist der seltenste Graphit, er bildet sich in Pegmatigängen und Spalten, in denen bei bereits relativ niedrigen Temperaturen von etwa 500–600 °C verschiedene Minerale kristallisieren. Seine Entstehung ist noch umstritten, jedoch gilt die Lösung von kohlenwasserstoffhaltigem Material in wässrigen Fluide mit anschließender Auskristallisation für am wahrscheinlichsten.[18]
Zugriffe - 1592
|
| H/C | First of all, you can identify the functional groups in biochar by FTIR analysis. If the spectrum reveals the evolution of aromatic functional groups replacing aliphatic groups of biomass, it shows the increase of aromatic Carbon in biochar. Also, you can use the Van Krevelen diagram. If H/C and O/C values decrease with the increase of pyrolysis temperature, it is an identification of increase of aromaticity in biochar.
Zugriffe - 1584
|
| Halbmetalle | Die Halbmetalle sind Elemente und stehen im Periodensystem zwischen den Metallen und den Nichtmetallen. Sie können von der elektrischen Leitfähigkeit und vom Aussehen her weder den Metallen noch den Nichtmetallen zugeordnet werden. Alle Halbmetalle sind Feststoffe bei Normalbedingungen. Halbleiter ist ein Überbegriff und umfasst Halbmetalle und Verbindungshalbleiter gleichermaßen.[1] Früher wurden Halbmetalle auch als Metalloide[2] bezeichnet, wobei diese Bezeichnung auch für Nichtmetalle verwendet wurde.[3][4]
Zugriffe - 1603
|
| Holzpreis m3 | 22.- bis 32.- /m3 10m3 /ha Ausbeute /Jahr
Zugriffe - 1652
|
| Hydrolyse | Die Hydrolyse ist formal gesehen die Spaltung einer chemischen Verbindung durch Reaktion mit Wasser. Formal wird bei der Reaktion ein Wasserstoffatom an das eine „Spaltstück“ abgegeben und die als Rest verbleibende Hydroxygruppe wird an das andere Spaltstück gebunden.
Zugriffe - 1587
|
| Hydrophil/Hydrophob | Wasserabstossend oder Wasserliebend Bei Temperaturerhöhung der Pyrolyse wird aus dem hydrophilen Material immer mehr ein hydrophobes.
Zugriffe - 1657
|
| Inega | Inega 200 kg C02/m3 Beton 2400 kg = 75 kg PK/m3
Zugriffe - 1601
|